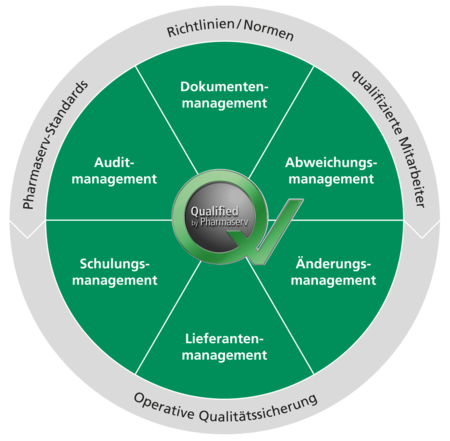
Dokumentenmanagement
Die Hierarchie der Pharmaserv Qualitätsdokumente klassifiziert sich in 4 Stufen.
- Kernprozesse (KP)
- Standard Betriebsanweisungen (SBA)
- Arbeitsanweisungen (AA)
- Formulare (FOR)
Alle Dokumente werden von dem Qualitätsmanagement Pharmaserv (QMP) gesteuert und überprüft. Spätestens alle drei Jahre werden bestehende Qualitätsdokumente turnusgemäß überprüft und bei Notwendigkeit, z. B. aufgrund gestiegener Qualitätsanforderungen optimiert.